Método de detección de lesión renal aguda
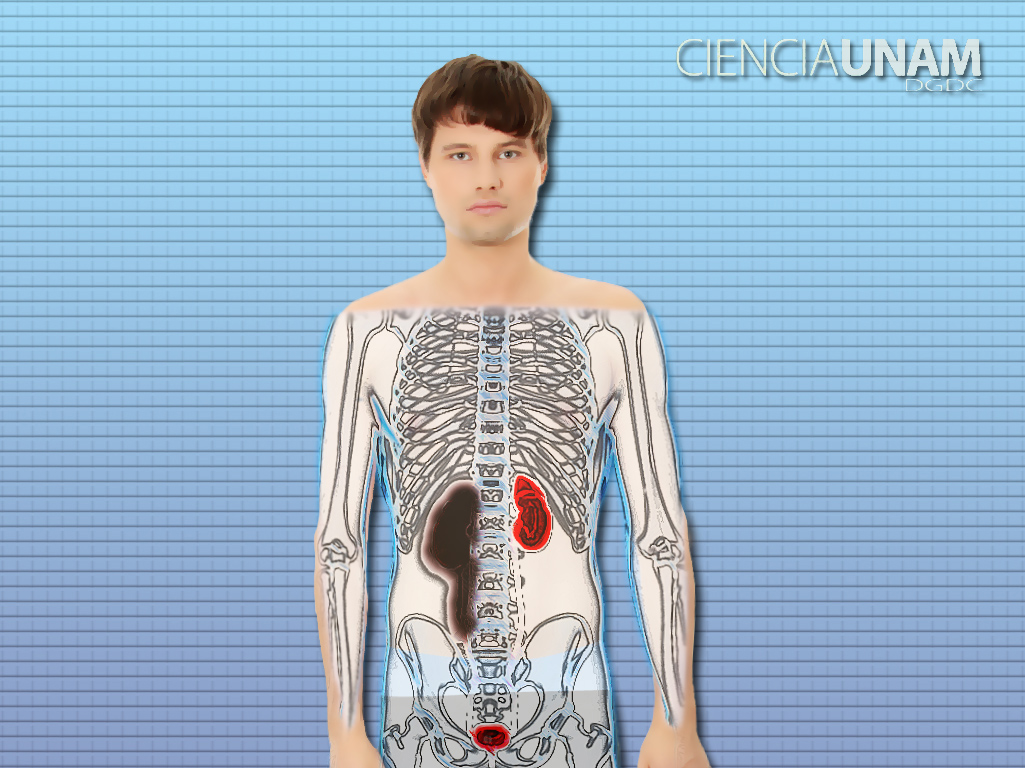
La lesión renal aguda se caracteriza por una caída del flujo sanguíneo renal. Diseño: Bárbara Castrejón.
04-07-2013
Por María Luisa Santillán, DGDC-UNAM
La lesión renal aguda (LRA) se presenta en pacientes sometidos a cirugías de alto riesgo, que se encuentran en terapia intensiva o en quienes recibirán algún medio de contraste para un estudio en particular, por ejemplo, quimioterapia con cisplatino. Aproximadamente entre el 5 y 10 por ciento de todos hospitalizados pueden padecerla y hasta el 50 por ciento de los ingresados a terapia intensiva pueden fallecer por esta causa.
La doctora Norma Bobadilla Sandoval, del Instituto de Investigaciones Biomédicas de la UNAM y del Instituto Nacional de Ciencias Médicas y Nutrición “Salvador Zubirán”, quien desde hace una década realiza estudios sobre este padecimiento, señaló que es importante encontrar tratamientos que prevengan la lesión renal aguda, pues se pensaba que una vez que ésta se resolvía, no había una consecuencia posterior; sin embargo, investigaciones recientes han mostrado que puede condicionar el desarrollo de enfermedad renal crónica.
En 2012, la investigadora universitaria ganó el premio Canifarma en la categoría de Investigación Tecnológica. Obtuvo el primer lugar por el trabajo La proteína de choque térmico de 72 kDa (Hsp72). El resultado de esta investigación fue la identificación de un biomarcador útil para la detección oportuna y la estratificación de lesión renal aguda. Asimismo, junto con sus colabores, busca desarrollar la creación de una tira reactiva para la detección inmediata de la enfermedad a través de la orina.
Aparición de la enfermedad
La LRA se caracteriza por una caída del flujo sanguíneo renal, es decir, llega menos oxígeno al tejido renal, siendo uno de los segmentos más dañados el epitelio tubular donde se forma la orina y el cual está ubicado después del glomérulo, lugar en que se realiza la filtración de la sangre. El segmento S3 del túbulo es el más dañado y se presenta muerte por necrosis y apoptosis.
Esta hipoxia, que lleva a la muerte celular, provoca que el epitelio empiece a regenerarse para continuar con su función normal, pero en algunas ocasiones o dependiendo de la intensidad del daño, las células epiteliales continúan proliferando inadecuadamente y esto trae como consecuencia que las células epiteliales produzcan TGF-beta, una citosina profibrótica que promueve más inflamación. La investigadora explicó que esto crea un círculo vicioso continuo de reparación, inflamación e hipoxia que tarde o temprano lleva al desarrollo de enfermedad renal crónica.
En la actualidad, se sabe que la aldosterona (hormona producida por las glándulas suprarrenales capaz de reabsorber sodio y secretar potasio) ejerce un efecto específico en las células del riñón, del túbulo distal y del túbulo conector, pero también se ha encontrado que puede ejercer efectos dañinos en otras células.
Resultados contundentes
Hace 10 años, en el laboratorio de la doctora Bobadilla Sandoval dio inicio una línea de investigación que arrojó como resultados la disminución de la nefrotoxicidad inducida por ciclosporina (medicamento utilizado para evitar el rechazo en el trasplante de riñón), además que no había vasoconstricción si la aldosterona era bloqueada.
Con este conocimiento y después de años de investigación, en 2007 se demostró que también en el daño renal producido por isquemia se evitaba la vasoconstricción y el riñón era mejor perfundido si la aldosterona era bloqueada.
Dos años después, en 2009, para demostrar que era la aldosterona quien estaba verdaderamente implicada en el daño renal, el grupo de investigación de la doctora Bobadilla Sandoval inició una nuevo protocolo, el cual consistió en quitar las glándulas suprarrenales de algunos animales de laboratorio con el fin de que no produjeran aldosterona y se protegieran contra el daño renal por isquemia.
“Y así fue: estos animales se protegieron por completo; no tuvieron disfunción renal, ni daño estructural. De esta manera probamos de forma contundente que la aldosterona es la que promueve mucho del daño por isquemia reperfusión”.
Asimismo, bajo la premisa de que entre 40 y 60 por ciento de los pacientes que ingresan a terapia intensiva presentan LRA de forma inesperada, junto con sus colaboradores trabajó en una nueva línea de investigación, en la cual evaluaron si administrar espironolactona después de que se inducía la isquemia también protegía a los animales de un daño renal.
“Observamos que si tratamos a los animales con espironolactona inmediatamente después y hasta seis horas posteriores de haber inducido isquemia, se protegen del desarrollo de lesión renal aguda. Nueve horas después, la protección fue mucho menor, por lo que entre más pronto intervenimos mejor es la aplicación. Esto nos permitió mostrar que la espironolactona es un tratamiento útil para prevenir enfermedades renales que estén relacionadas con un proceso isquémico como sucede con la nefrotoxicidad por ciclosporina, por isquemia reperfusión y por algunos fármacos que tienen que ver con alguna reducción del flujo sanguíneo”, explicó.
Con estas observaciones, un siguiente paso fue saber si al prevenir la lesión renal aguda se previene el desarrollo de enfermedad renal crónica. Estudios recientes de la investigadora mostraron que si se producía isquemia en los animales y no se les daba ningún tratamiento, nueve meses después desarrollaban enfermedad renal crónica severa, pero si se bloqueaban las acciones de la aldosterona se protegían por completo de dicho padecimiento.
Una aplicación clínica
El grupo de investigación de la doctora Norma Bobadilla Sandoval ha iniciado dos estudios clínicos. Uno en el Hospital Infantil de México, en conjunto con la doctora Mara Medeiros, con quien trabaja en un protocolo con niños que padecen nefrotoxicidad por ciclosporina. Otro es en el INCMNSZ, con el doctor Luis Eduardo Morales, con pacientes que recibirán un trasplante de riñón.
Por último, la investigadora comentó que es importante encontrar los mecanismos a nivel molecular de la lesión renal aguda, desarrollar nuevas terapias que permitan bloquear la acción de la aldosterona, así como prevenir la aparición de la enfermedad renal crónica, además de que se debe buscar dirigir la investigación básica en beneficio de los pacientes.
Publicaciones relacionadas

Detección oportuna de lesiones en riñón, prioridad de Norma Bobadilla

Esterilización: método para reducir la población de perros y gatos en las calles
Innovador biosensor aplicado a la detección de la vaginosis bacteriana